Tecnologia medica di sicurezza La sicurezza come massima
Gestione del rischio secondo DIN EN ISO 14971
La sicurezza di pazienti, medici e infermieri è di grande importanza per Interelectronix .
Con l'introduzione di un sistema di gestione dei rischi per i dispositivi medici secondo DIN EN ISO 14971, siamo più che all'altezza della nostra massima.
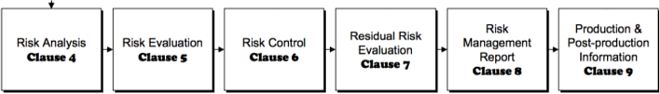
Indipendentemente dalle normative legali, l'applicazione della gestione del rischio dall'idea del prodotto al lancio sul mercato è costantemente praticata a Interelectronix in tutti i processi e reparti e comprende i seguenti componenti:
-Analisi del rischio
-Valutazione del rischio
- Controllo del rischio
- Analisi delle informazioni rilevanti per il rischio derivanti dall'osservazione del mercato
- Valutazione delle lezioni apprese dal processo di gestione del rischio
Un elemento importante della nostra gestione del rischio è una rivalutazione periodica di tutte le misure dopo che sono state implementate. Tuttavia, questo non si esaurisce con la consegna di un prodotto, ma include specificamente l'osservazione del mercato del prodotto durante le sue fasi del ciclo di vita.
Se necessario, viene effettuato un adeguamento dinamico della gestione del rischio per i dispositivi medici attraverso un'attenta osservazione dei prodotti e delle loro funzioni in uso, tenendo conto dei rispettivi tipi di pericolo.
I prodotti di tecnologia medica devono essere sicuri ed efficienti da usare. Di conseguenza, è logico applicare la gestione del rischio già nella fase di sviluppo.
L'obiettivo primario della gestione Interelectronix del rischio è quindi quello di garantire l'eliminazione o la minimizzazione dei rischi attraverso misure concettuali o costruttive.
Questo inizia con la progettazione di un prodotto e si estende a tutti i processi, le procedure e le procedure di produzione.
L'analisi del rischio è una parte importante della gestione del rischio
L'esecuzione di un'analisi del rischio è richiesta dalle procedure di approvazione nell'UE e dalla FDA. È un modo efficace per indirizzare gli sforzi di sviluppo e convalida del prodotto dove possono sorgere i maggiori rischi.
La Failure Mode and Effects Analysis (FMEA) è stata finora una componente essenziale della garanzia della qualità prima dell'inizio della produzione in serie. Tuttavia, le analisi dei rischi secondo DIN EN ISO 14971 differiscono notevolmente dalla FMEA.
L'analisi delle modalità e degli effetti di guasto non è quindi più riconosciuta dagli enti omologanti per l'omologazione dei dispositivi secondo EN 60601-1 3a Edizione.
MOPP - Mezzi di protezione del paziente
La norma IEC 60601-1 definisce "Mezzi di protezione del paziente (MOPP) per ridurre il rischio di scosse elettriche per il paziente".
Di conseguenza, i dispositivi medici devono sempre essere dotati di due misure di protezione indipendenti per la protezione del paziente al fine di essere "primi a prova di guasto".
Se una delle due misure di protezione fallisce, la sicurezza del paziente non deve essere compromessa. A seconda del tipo di pericolo, diversi sistemi di protezione di solito lavorano fianco a fianco, che hanno lo scopo di contrastare diversi potenziali di pericolo.
-Dielettrica
Un'elevata rigidità dielettrica ha lo scopo di proteggere dalle sovratensioni pulsate che si verificano frequentemente nei sistemi elettrici.
Struttura isolante specifica per l'applicazione
Una struttura isolante specifica per l'applicazione ha lo scopo di prevenire il rischio di isolamento inadeguato a causa di difetti di fabbricazione o del processo di invecchiamento.Distanza di gioco e dispersione
Ambienti umidi o polverosi possono portare a flashover elettrici, che dovrebbero essere evitati mediante distanze di gioco e dispersione.Correnti di dispersione - correnti di dispersione
I pazienti devono essere protetti dalle correnti di dispersione agenti riducendole ai valori massimi delle correnti di dispersione (lo standard dipende dal dispositivo).Connessioni conduttori di protezione
Le connessioni dei conduttori di protezione sono progettate per dissipare le correnti pericolose in modo che non raggiungano il paziente.Corrente di dispersione paziente (DIN 60479-1)
La corrente di dispersione del paziente viene creata da un circuito elettrico impeccabile nel dispositivo, che scorre direttamente attraverso il conduttore di protezione o indirettamente come corrente di dispersione del dispositivo tramite parti conduttive del dispositivo a terra, rappresentando così un pericolo per i pazienti.
Sistemi touch e HMI secondo lo standard IEC/UL 60601-1
Soprattutto nella tecnologia medica, la sicurezza dei dispositivi, la protezione personale, l'elevata igiene, la lunga durata, l'affidabilità e l'integrazione funzionale efficiente sono della massima importanza. Tutti i touch panel e i sistemi touch sviluppati da Interelectronix sono soggetti agli elevati requisiti di sicurezza per i dispositivi medici in conformità con la norma di base IEC/UL 60601-1.
La norma IEC/UL 60601-1 definisce i requisiti generali per le caratteristiche di sicurezza di base e le prestazioni essenziali dei sistemi elettromedicali collegati a una rete di alimentazione destinati alla diagnosi, al trattamento o al monitoraggio di un paziente. La norma europea EN 60601-1 è identica alla norma IEC/UL 60601-1.
Grazie alla loro elevata affidabilità e tecnologia avanzata, al loro design innovativo del prodotto e all'usabilità intuitiva, i sistemi touch Interlecronix sono utilizzati da
- Dispositivi ad ultrasuoni
- Macchine a raggi X
- Scanner per tomografia computerizzata
- Apparecchiature per analisi di laboratorio
così come
- in sala operatoria
- in odontoiatria
- nel monitoraggio dei pazienti
- e registrazione del paziente
usato.
Nel caso dei touchscreen utilizzati nella tecnologia medica, la corrente di dispersione del paziente può essere evitata con un design specifico, l'isolamento o l'uso di materiali adatti come alloggiamenti in plastica o pannelli frontali.
Ogni pannello a sfioramento utilizzato nella tecnologia medica è soggetto a un controllo preciso del flusso di corrente esatto per rilevare ed evitare la corrente di dispersione del dispositivo.
Test di protezione secondo IPX1 a IPX8
I touchscreen nei dispositivi medici sono soggetti a requisiti di sicurezza particolarmente elevati. Ad esempio, i sistemi touch devono spesso funzionare senza errori per anni in condizioni difficili e allo stesso tempo garantire una protezione completa per i pazienti e il personale operativo.
I touchscreen utilizzati nella tecnologia medica sono soggetti a una notevole esposizione a detergenti, disinfettanti, acqua, vapori, acidi o fluidi corporei. Inoltre, l'ingresso di corpi estranei e polvere, così come la contaminazione con batteri e virus, devono essere praticamente eliminati.
In base ai rispettivi requisiti e campi di applicazione, Interelectronix sviluppa sistemi touch pronti per l'installazione conformi alle varie classi di protezione e standard da IPX1 a IPX8:
- Protezione contro corpi estranei (DIN 40 050 parte 9 o DIN EN 60529)
- Protezione contro l'acqua (DIN 40 050 parte 9 o DIN EN 60529, test di classe di protezione dell'acqua)
- Resistenza agli urti (DIN EN 62262)
In qualità di specialista di sistemi touch di alta qualità e pronti per l'installazione, Interelectronix vanta molti anni di esperienza nello sviluppo di touchscreen, touch panel e sistemi touch completi che soddisfano i requisiti speciali della tecnologia medica per la sicurezza, la durata e la protezione del paziente.
Una vasta gamma di vetri, materiali di alloggiamento, guarnizioni di alta qualità e tecniche di laminazione consentono la costruzione di HMI (Human Machine Interface) conformi a IPX1 a IPX8.